NIR-II 荧光成像引导的光热/化学/抗血管生成疗法的纳米
本文要点:最近,实时光学成像和光控制治疗相结合的光热疗法已成为一种很有前途的癌症治疗疗法范例。本文设计并成功合成了一种1000 nm以上的小分子染料DPP-BT-TPA和一种基于氧化还原反应的前药——喜树碱联合血管生成抑制素A4(CPT-CA4),将其封装在两亲性聚合物中,制备了一种多功能的光疗纳米平台。该前药CPT-CA4在肿瘤微环境中被过表达的谷胱甘肽(GSH)裂解,释放化疗药物CPT和血管生成抑制剂CA4。这一过程可以随着高温而加速,且可以利用NIR-II成像观察活小鼠的肿瘤。通过光热/化疗/抗血管生成组合提高了抗肿瘤疗效。
背景:NIR-II荧光成像能对深度组织进行清晰且高分辨的成像,最近已成为光学成像中前所未有的技术。小分子具有明确的化学结构、较高的合成重现性、良好的生物安全性和快速的代谢,成为最有前途的候选分子。但是小分子的Stokes位移较短和稳定性较差在很大程度上限制了它们的应用。因此,开发具有长斯托克斯位移和高稳定性的新型NIR-II发射小分子对于光热学领域是非常有价值的。光热疗法通过光照射局部产生的热量来消融肿瘤,而不依赖于周围的微环境。但是,PTT也存在一些棘手的问题,如穿透深度有限,肿瘤复发,以及可能损害正常组织。而化疗作为在临床环境中治疗癌症最有效的手段之一,许多化疗药物如阿霉素、喜树碱和顺铂可尝试与PTT联合使用,以增强光热治疗系统的治疗效果。
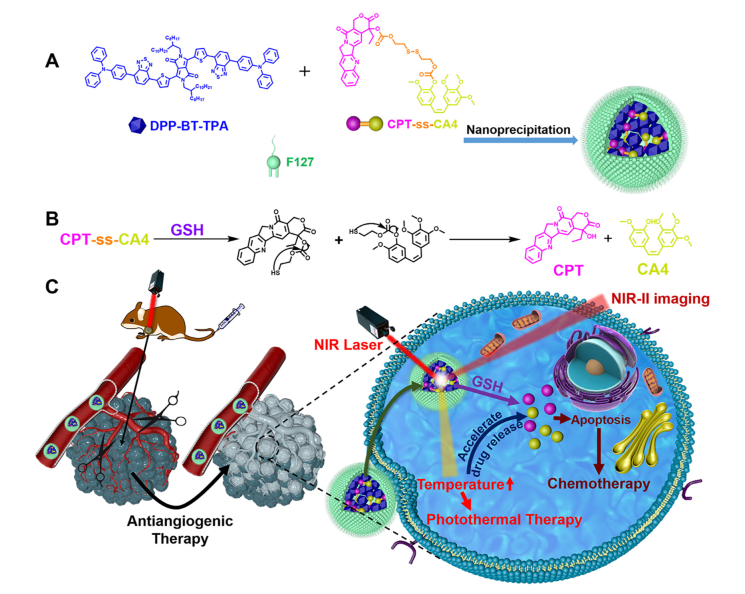
研究内容:本文设计并合成了一种基于二酮吡咯(DPP)的小分子DPPBT-TPA,在1000 nm以上具有强发射能力,在730 nm照射下具有优越的光热性能。然后将DPP-BT-TPA与喜树碱CA4相连的前药(CPT-ss-CA4)共封装在两亲性聚合物胶束中,制备了一个单一激光触发的光疗平台,再利用谷胱甘肽(GSH)裂解前药,释放化疗药物CPT和血管生成抑制剂CA4。在激光照射下,光热效应大大加速了这一过程。(Fig.1)
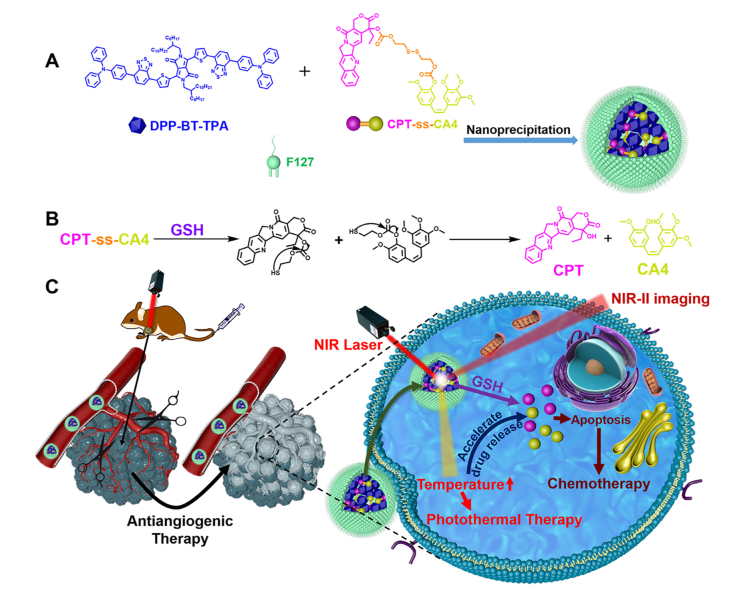
Figure 1
利用两亲性聚合物F-127包封DPP-BT-TPA,通过纳米沉淀法制备水溶性DPP-BT-TPA NPs(Fig.2A-B),得到的NPs具有较高的胶体稳定性。该纳米探针在640 nm左右出现了一个吸收峰(Fig.2C),利用730 nm激发,NPs在1000nm处出现较强的NIR-II区发射,表现出长Stokes位移。此外,DPP-BT-TPA NPs在激光照射下表现出较高的光稳定性,优于商业染料ICG(Fig.2D)。
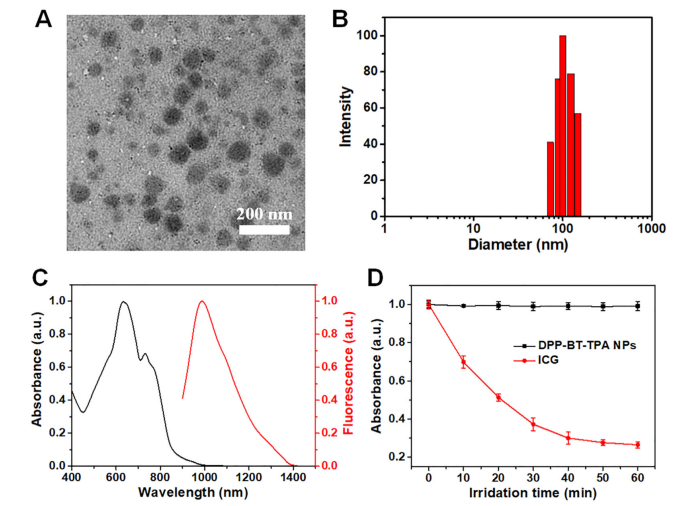
Figure 2
如Fig.3A所示,在激光照射后,DPP-BT-TPA NPs溶液的温度显著升高,且呈浓度依赖性。最高温度达到62°C。DPP-BT-TPA NPs也表现出较高的光热稳定性。在四个开关循环中,溶液温度达到了几乎相同的值(Fig.3C)。DPP-BT-TPA NPs的光热转换效率为44.3%(Fig. 3D)。
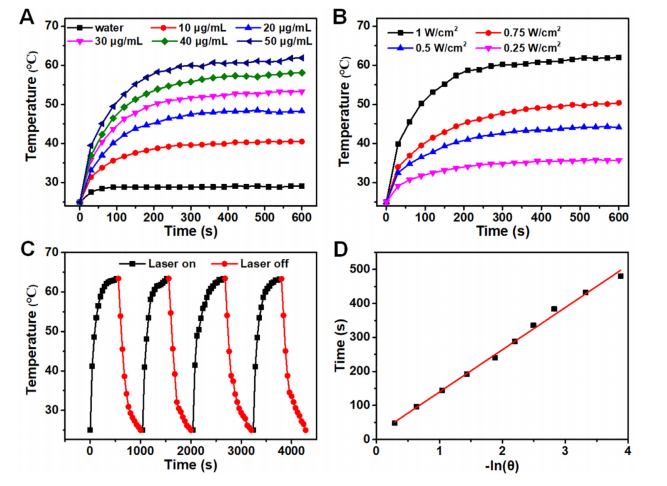
Figure 3
之后作者将DPP-BT-TPA和CPT-ss-CA4封装在聚合物F127中,得到一个纳米治疗体系DCssC NPs(Fig.4A-C)。可通过监测DCssC NPs的体外药物荧光发射强度,记录其体外药物释放情况。从Fig.4E-G可知,药物的释放依赖温度,更高的温度下药物释放更快,因此,利用730 nm激光诱导的DPP-BT-TPA的光热效应可以用来控制CPT和CA4的释放。
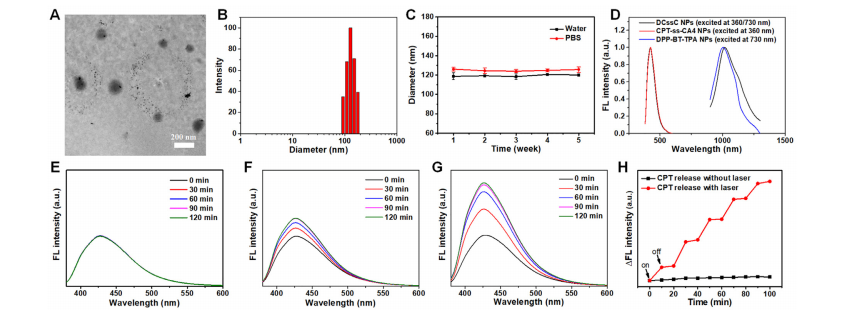
Figure 4
采用MTT法检测DPP-BT-TPA NPs和DCssC NPs对癌细胞的体外细胞毒性(Fig.5A),DPP-BT-TPA NPs和DCssC NPs在730 nm激光照射后具有显著的细胞毒性,PI染色下有更多的红色荧光表明DCssC NPs组的细胞死亡率更高。(Fig.5B)。
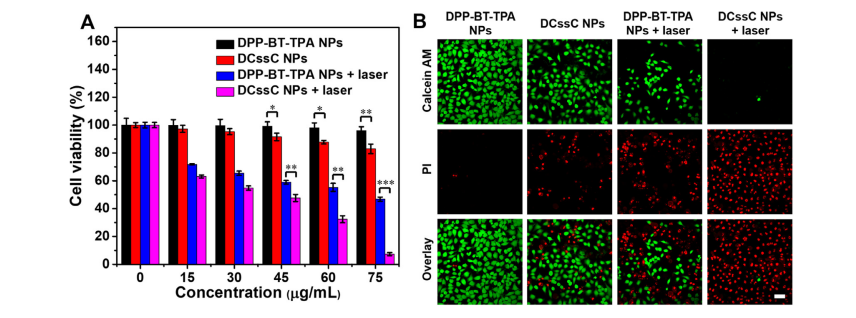
Figure 5
体内成像实验表明,肿瘤区域的NIR-II荧光信号随时间逐渐增加,并在注射后12 h达到最大值(Fig.6A)。纳米探针主要分布在肝,脾和肿瘤(Fig.6B-6D)。DCssC NPs通过EPR作用在肿瘤中积累,并通过肝胆系统代谢。
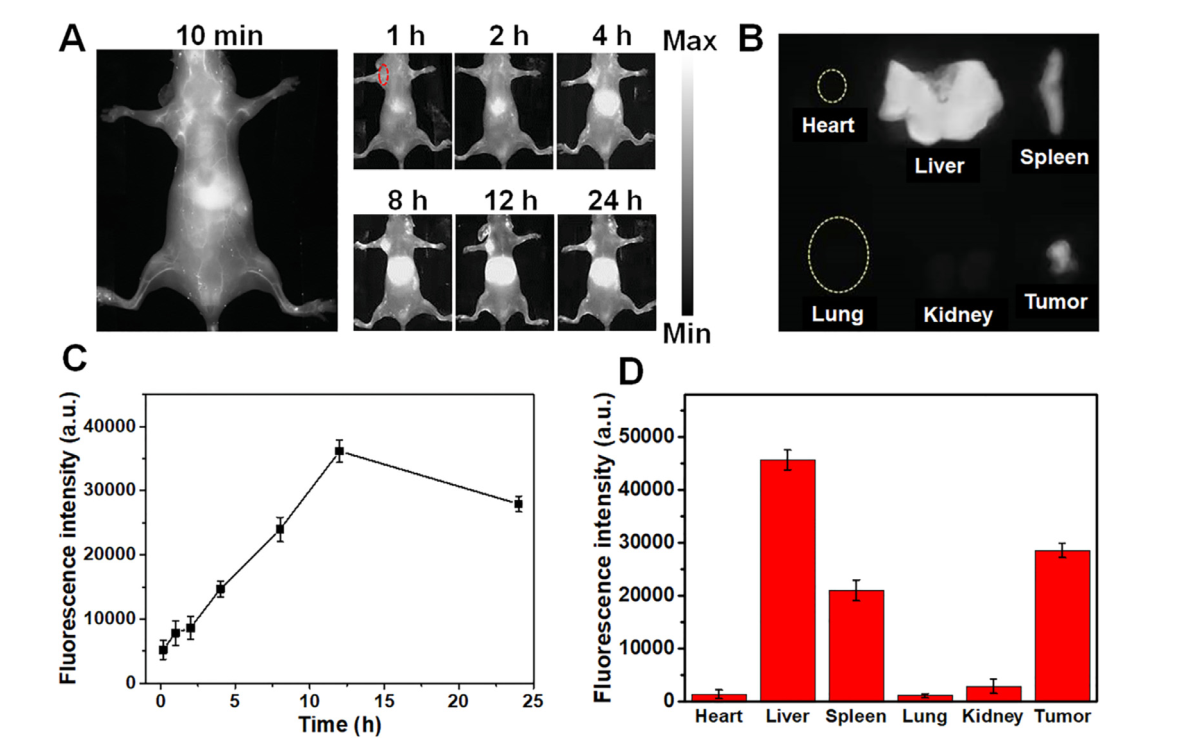
Figure 6
在注射纳米探针12 h后,从Fig.7A可发现,肿瘤区域的温度达到52°C左右。每两天测量一次肿瘤体积和体重。DPP-BT-TPA NPs+激光照射组的肿瘤抑制效果最高。而各组的体重差异较小(Fig.7B-7C),说明所制备的纳米探针在激光下可抑制肿瘤生长,而且副作用较小。进一步采用H&E染色法评价DCssC NPs在体内的毒性,表明各组治疗后主要器官均无明显病变(Fig.7D)。
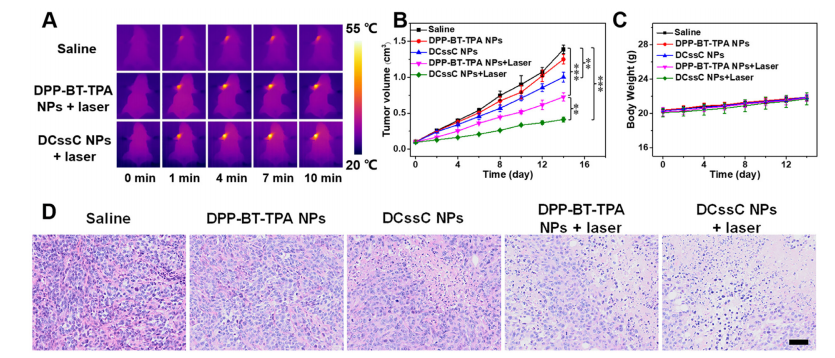
Figure 7
总结:作者成功制备了一种具有高光热转换效率、良好生物相容性的新型NIR-II发射小分子染料DPP-BTTPA。通过连接化疗药物喜树碱和血管生成抑制剂A4,也获得了GSH-可裂解的前药CPT-ss-CA4。DPP-BT-TPA和CPT-ss-CA4被封装在两亲性聚合物F-127中,从而产生了一种新的光热剂(DCssC NPs),用于NIRII成像引导下的光热治疗、抗血管生成治疗和化疗。
参考文献
doi.org/10.1016/j.actbio.2022.08.013
⭐️ ⭐️ ⭐️
近红外二区小动物活体荧光成像系统 - MARS
NIR-II in vivo imaging system

高灵敏度 - 采用Princeton Instruments深制冷相机,活体穿透深度高于15mm
高分辨率 - 定制高分辨大光圈红外镜头,空间分辨率优于3um
荧光寿命 - 分辨率优于 5us
高速采集 - 速度优于1000fps (帧每秒)
多模态系统 - 可扩展X射线辐照、荧光寿命、一区荧光成像、原位成像光谱,CT等
显微镜 - 近红外二区高分辨显微系统,兼容成像型光谱仪
⭐️ ⭐️ ⭐️
恒光智影
上海恒光智影医疗科技有限公司,专注于近红外二区成像技术。致力于为生物医学、临床前和临床应用等相关领域的研究提供先进的、一体化的成像解决方案。自主研发近红外二区小动物活体荧光成像系统-MARS。
与基于可见光波长的传统成像技术相比,我们的技术侧重于X射线、紫外、红外、短波红外、太赫兹范围,可为肿瘤学、神经学、心血管、药代动力学等一系列学科的科研人员提供清晰的成像效果,助力科技研发。
同时,恒光智影还具备探针研发能力,我们已经成功研发了超过15种探针,这些探针将广泛地应用于众多生物科技前沿领域的相关研究中。
全部评论(0条)
推荐阅读
-
- 用户文章丨《Pediatr Blood Cancer.》王华教授团队应用超快三维荧光成像取得婴儿血管瘤临床检测标志物研究最新成果
- 重庆医科大学附属儿童医院王华教授团队应用长光辰英核心产品S3000超快三维荧光成像系统在《Pediatric Blood \x26amp; Cancer》期刊上发表了文章
-
- 热点应用丨复旦大学张凡团队开发近红外二区新型稀土荧光探针用于实时动态的活体多重荧光成像
- 复旦大学张凡教授团队开发了近红外第二窗口新型稀土荧光探针以及双通道实时成像技术
-
- 植物叶绿素荧光成像系统
- 广泛应用于植物学、农学、林学、环境科学等植物相关领域,有助于进行植物生长、胁迫、育种、突变株筛选等相关学科光合研究,用于植物生理生态及表型研究。
-
- 【文献速递】肿瘤微环境响应的分子工程纳米平台可以实现NIR-II荧光成像的组合癌症治疗
- 回复“试用”可免费试用文献同款仪器!
-
- 热点应用丨复旦大学张凡团队开发开发近红外第二窗口长余辉探针实现高信噪比活体成像
- 荧光成像由于具有非侵入性、高灵敏度、高时空分辨率等优点,被广泛用于生命科学和临床医学等领域。
①本文由医疗器械网入驻的作者或注册的会员撰写并发布,观点仅代表作者本人,不代表医疗器械网立场。若内容侵犯到您的合法权益,请及时告诉,我们立即通知作者,并马上删除。
②凡本网注明"来源:医疗器械网"的所有作品,版权均属于医疗器械网,转载时须经本网同意,并请注明医疗器械网(www.120med.com)。
③本网转载并注明来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
④若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi





参与评论
登录后参与评论